特價熱銷 可愛忍者兔中性筆,日韓文具之選
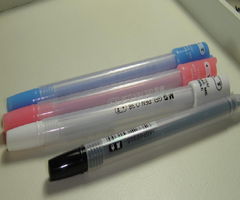
在當今文具市場中,日韓風格的文具因其獨特的設計和實用性備受歡迎。特此推出特價熱銷產品——日韓可愛忍者兔中性筆卡通水筆,每支僅重8g,輕便易攜,是文具用品批發的理想選擇。
這款中性筆以可愛的忍者兔形象為主題,融合了日本和韓國的卡通設計元素,色彩鮮艷,線條流暢,不僅吸引了兒童和青少年的喜愛,也深受成年文具愛好者的青睞。筆身采用環保材質,安全無毒,書寫流暢,墨水均勻,適合日常學習、辦公和繪畫使用。
作為文具用品批發,我們提供批量采購優惠,價格實惠,滿足學校、書店、禮品店等各類商家的需求。產品包裝精美,可定制logo,是促銷活動和節日禮品的絕佳選項。忍者兔中性筆輕巧的設計便于庫存管理,8g的輕量級規格減少運輸成本,提升批發效率。
這款日韓文具可愛忍者兔中性筆不僅外觀吸睛,功能實用,還能通過批發渠道帶來可觀利潤。歡迎廣大商家咨詢訂購,共享文具市場的熱銷浪潮。
如若轉載,請注明出處:http://www.499406.com.cn/product/1.html
更新時間:2026-01-25 17:31:08









